החלבונים "שמדברים" רק עם מי שאנחנו רוצים
המחקר שנערך באוניברסיטת חיפה עשוי להוביל למניעת תופעות לוואי, שנגרמות מנטילת תרופות. מוביל המחקר: "הממצא שלנו משפר את היכולת למצוא בעתיד את הדרך להפעיל בכל פעם אך ורק את החלבונים הספציפיים ואת המנגנון המסויים שאנחנו רוצים"
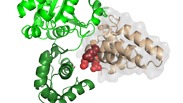
חוקרים באוניברסיטת חיפה הצליחו לפענח את הקוד המולקולארי, שמאפשר לחלבונים לתקשר באופן ספציפי עם חלבונים אחרים, כחלק משרשראות של תקשורת תאית. אחת המשמעויות של המחקר, שפורסם בכתב העת Journal Of Molecular Biology, היא שההבנה כיצד לתקשר באופן פרטני עם חלבון בודד תאפשר פיתוח תרופות עם פחות תופעות לוואי בשלל מחלות כמו סרטן, מחלות לב ועוד.

ד"ר מיקי קוזלוב מהחוג לביולוגיה של האדם באוניברסיטת חיפה, שהוביל את המחקר, אמר: "אחת הבעיות בפיתוח תרופות היא שתרופה מפעילה לא רק את התהליך שרצינו, אלא גם תהליכים נוספים שלא רצינו להפעיל, ובכך הנזק גדול מהתועלת. הממצא שלנו משפר את היכולת שלנו למצוא בעתיד את הדרך להפעיל בכל פעם אך ורק את החלבונים הספציפיים ואת המנגנון המסויים שאנחנו רוצים".
.
תהליך של תקשורת תאית הוא תהליך שבו חלבון, או קבוצה של חלבונים, נקשרים לחלבונים אחרים שנמצאים בתוך התא - ובכך מפעילים רשת תקשורת תוך תאית. רשתות כאלה שולטות על כל התהליכים בגוף כגון חישה, בקרה הורמונלית, פעילות עצבית ועוד. תקלות בתקשורת התאית גורמת למחלות קשות, כך לדוגמה, במחלת הסרטן, "תקלה" בתקשורת התאית גורמת לתאים "לאבד" את השליטה על קצב החלוקה והמוות הטבעי, ולהתחלק ללא הפסקה.
החוקרים הסבירו כי חלבוני G וחלבוני RGS הם חלבונים שלוקחים חלק משמעותי במנגנוני התקשורת הבין-תאית באזורים רבים בגוף ולכן הם משמשים כמודל טוב לפענוח הבסיס המולקולרי לתקשורת תאית באופן כללי, ולפענוח הקוד הקובע את ההידברות בין חלבונים באופן פרטני. חלבוני G הם מתגים מולקולאריים: כאשר התא נחשף לגירוי המפעיל את התקשורת התאית, חלבוני ה-G הם המפעילים את שרשרת הפעולות שבאה אחריהם. תפקידם של חלבוני ה-RGS הוא לכבות מתגים מולקולאריים אלה ולבלום הפעלה חזקה מדי או ארוכה מדי של רשתות התקשורת בתא.
בגוף האדם סוגים רבים של חלבוני G כשלעיתים יש הבדלים קטנים מאוד בין חלבון לחלבון. כשרוב חלבוני ה-RGS מופעלים הם מכבים במקביל מספר רב של חלבוני G, כלומר: הם לא יודעים להבחין בין הסוגים השונים של חלבוני G. אולם יש מספר מצומצם של חלבוני RGS שיודעים להבחין בין הסוגים השונים ויודעים לכבות חלבון G ספציפי, מבלי לכבות חלבוני G שונים סמוכים.
במחקר הנוכחי הצליחו ד"ר קוזלוב, יחד עם תלמידי המחקר רן ישראלי ועלי עסלי והחוקרת ד"ר מירב אביטל-שחם, להבין כיצד פועלים חלבוני ה-RGS הללו באופן מדויק. לשם כך, הם התמקדו בפעילות של החלבונים RGS6 ו-RGS7 - שיודעים להבחין בין החלבון Gαi והחלבון Gαo. חלבוני G אלה נפוצים ברגולציה של תקשורת תאית בלב ובמוח ונקשרו במחקרים קודמים לחרדה ודיכאון, בעיות בקצב הלב ועוד.
החוקרים גילו כי בעוד שאצל חלבוני RGS "רגילים" פועלת קבוצה אחת של חלבוני אמינו, שאחראית על חיזוק הקשר התאי, בקרב חלבוני ה-RGS "המדויקים" פעילה קבוצה נוספת של חומצות אמינו שאותה גילתה המעבדה של ד"ר קוזלוב במחקרים קודמים. אותה קבוצה דווקא מחלישה את הקשר התאי. לעומת זאת, במחקר הנוכחי נמצאה קבוצה שלישית של חומצות אמינו שפעילה רק בקרב החלבונים "המדויקים". כך שבקרב קבוצה זו של חלבונים, ובשונה מחלבוני ה-RGS "הרגילים", פועלות שלוש קבוצות של חומצות אמינו. במחקר הנוכחי גם גילו החוקרים את היחס המדוייק בין קבוצות חומצות אמינו אלו שמבדילות בין יכולות הדיוק של RGS6 ו-RGS7 ליתר חלבוני ה-RGS "המדויקים".
ד"ר קוזלוב אמר כי הבנת תהליך התקשורת התאית היא לא רק מפתח להבנת הפעילות וה"תקלות" בגוף האנושי, אלא גם בעלת משמעות מרחיקת לכת לתעשיית התרופות. זאת, מכיוון שכשליש מהתרופות הקיימות כיום בשוק מתערבות בתהליך התקשורת התאית המתווכת על ידי חלבוני ה-G. "למעשה, למעלה מ-90% מהתרופות שנכנסות לתהליך של פיתוח עבור חולים נפסלות בגלל תופעות לוואי קשות מדי. כלומר, אין לנו את הכלים לפתח מראש תרופה שתדע להפעיל חלבונים ספציפיים ולכן אולי הפעלנו את המנגנון התאי שרצינו, אבל גם שורה של מנגנונים נוספים שלא רצינו שיופעלו. בזכות המחקר הנוכחי עשינו צעד נוסף בהבנה כיצד להפעיל אך ורק את המנגנון שאותו אנחנו רוצים להפעיל וכך כמובן נדע לפתח תרופות עם פחות ופחות תופעות לוואי".