פרס נובל ברפואה או פיזיולוגיה יוענק לשני ביולוגים אמריקנים, פרופ' ויקטור אמברוז ופרופ' גארי רובקון (היהודי), על גילוי מיקרו-RNA - מולקולות RNA קטנות. כך הוכרז בצהריים (יום ב') בשטוקהולם. התגלית שלהם ב-1993 זיכתה את שניהם בפרס וולף הישראלי לפני עשור יחד עם החוקר הישראלי-קנדי פרופ' נחום זוננברג. פרופ' זוננברג לא קיבל את פרס נובל, למרות שלעתים קרובות ועדת הפרס בשטוקהולם מעניקה את פרס נובל לשלושה חוקרים בשנה בכל תחום. ynet העביר את ההכרזה בשידור חי.
הכרזת זוכי הנובל ברפואה לשנת 2024
פרס נובל ברפואה מוכרז על-ידי מכון קרולינסקה השבדי, כחודשיים לפני טקס הענקת הפרסים. סכום הפרס עומד על 11 מיליון קרונות שבדיות שהם כארבעה מיליון שקל.
פרופ' רובקון (Ruvkun) מבית החולים הכללי של מסצ'וסטס ואוניברסיטת הרווארד ופרופ' אמברוז (Ambros) מאוניברסיטת מסצ'וסטס גילו את תפקידן של המולקולות הקטנות ב-1993, ותפקידן בבקרה על ביטוי גנים – כלומר על התהליכים שמובילים לייצור החלבון המקודד בגֵנים מסוימים. מנגנון המיקרו-RNA מבוסס על רצפים קצרים מאוד של החומר הגנטי, והוא אחד המנגנונים שמאפשרים לכל תא לייצר חלבונים שונים, אף על פי שהחומר התורשתי זהה בכולם.
3 צפייה בגלריה


מימין לשמאל: פרופ' גארי רובקון ופרופ' ויקטור אמברוז, זוכי נובל ברפואה
(צילום: Steve Jennings/Getty)
הגנום שלנו, המורכב ממולקולות ה-DNA שבגרעיני התאים שלנו, הוא מעין ספר הוראות עצום, שעל פיו מיוצרים ומורכבים כל החלבונים שבגופנו. כמעט בכל תא יש לנו עותק של ה"ספר" השלם, אותן הוראות לבנייה של כל החלבונים. אבל כמובן, לא כל תא מייצר את כל אותם החלבונים. בתא שריר מיוצרים חלבונים שמרכיבים סיבים המסוגלים להתכווץ, ברשתית העין – חלבונים שמשנים את צורתם בתגובה לאור, בתאי עצב חלבונים שמאפשרים העברת אותות חשמליים, וכך הלאה בכל סוגי התאים הרבים בגופנו.
איך תא יודע שעליו להיות תא שריר, למשל, ולייצר חלבונים בהתאם? זוכי הפרס השנה חשפו את אחד המנגנונים שמבטיחים שכל תא ייצר רק את החלבונים המתאימים לסוג שלו. המולקולות שגילו הם מקטעים קטנים של RNA, המכונים מיקרו-RNA, והם משמשים בבקרה על ייצור החלבונים.
פרסי נובל מוענקים מדי שנה ב-10 בדצמבר, יום השנה למותו של אלפרד נובל, מייסד קרן הפרס. הפרסים מוענקים בתחומי רפואה או פיזיולוגיה, פיזיקה, כימיה, ספרות ושלום. לאחר הכרזת פרס נובל ברפואה יוכרזו בימים הבאים יתר הזוכים. מ-1969 מוענק גם פרס בכלכלה על שם אלפרד נובל, וזה גם הפרס שיחתום את שרשרת הכרזות הנובל בעוד שבוע בדיוק. ביום שישי יוכרז באוסלו הזוכה בפרס נובל לשלום.
מה רוצה התולעת?
RNA הוא חומצת גרעין, ודומה בהרכבו ל-DNA, שממנו בנויים הגנים שלנו. ה-RNA המוכר ביותר הוא RNA שליח, שתפקידו לתווך בין הגרעין, שבו נמצא ה-DNA, לריבוזום, המכוֹנה שמייצרת את החלבונים מחוץ לגרעין התא. גֵן הוא רצף הוראות לבניית חלבון: כדי לבנות את החלבון התא מייצר מולקולת RNA שליח שמעתיקה את ההוראות הכתובות בגֵן, בתהליך שנקרא שעתוק. על פי ה-RNA הריבוזום בונה את החלבון.
כבר בשנות ה-60 של המאה ה-20 גילו חוקרים שיש חלבונים מיוחדים שמסוגלים להשפיע על רמת הביטוי של חלבונים אחרים, כלומר אם, וכמה מהם, יווצרו בתא מסוים. הם זכו לשם גורמי שעתוק (transcription factors), כי הם השפיעו על הסיכוי שגֵן מסוים יעבור שעתוק ל-RNA שליח, ובסופו של דבר התא ייצר על פיו את החלבון. חלבונים כאלו נצמדים למקומות מסוימים ב-DNA, ומאפשרים או מונעים את יצירת ה-RNA.
"במשך שנים רבות ההשערה הרווחת הייתה שהחלבונים הללו הם הגורם העיקרי שמווסת את ייצור החלבונים בתאים השונים. אמברוז ורובקון הראו שזה לא המנגנון היחיד - הם גילו את מולקולות המיקרו-RNA"
במשך שנים רבות ההשערה הרווחת הייתה שהחלבונים הללו הם הגורם העיקרי שמווסת את ייצור החלבונים בתאים השונים. אמברוז ורובקון הראו שזה לא המנגנון היחיד - הם גילו את מולקולות המיקרו-RNA.
בסוף שנות השמונים אמברוז ורובקון שהו יחד בהשתלמות פוסט-דוקטורט במכון הטכנולוגי של מסצ'וסטס (MIT), במעבדה של רוברט הורביץ (Horvitz), לימים חתן פרס נובל ברפואה בעצמו (2002). אמברוז, שנולד בקליפורניה ב-1952 הגיע לשם אחרי דוקטורט באוניברסיטת הרווארד הסמוכה, ואילו אמברוז, שנולד ב-1953 בניו המפשייר, נשאר ב-MIT אחרי שסיים שם את הדוקטורט ב-1979.
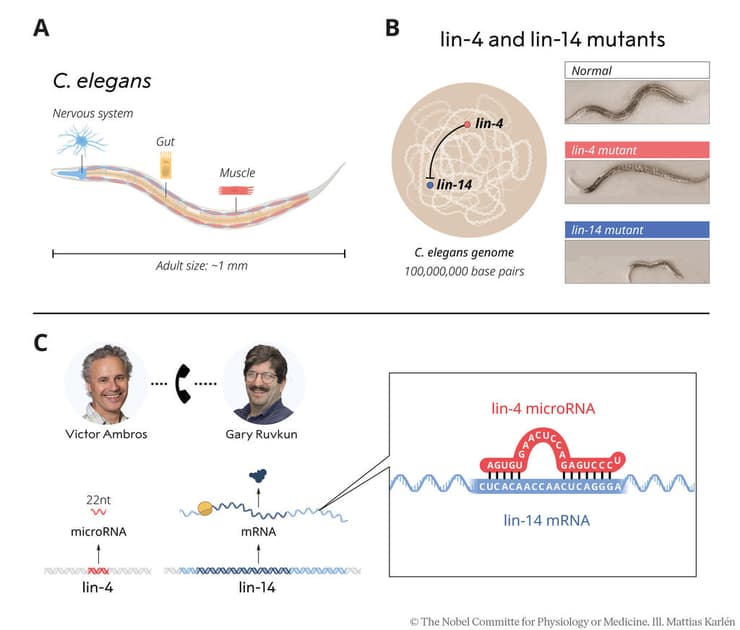
הם עשו שם את המחקר בנמטודות, תולעים עגולות זעירות, מהמין C. elegans, המשמשות חיות מודל למחקרים רבים בגנטיקה, וחיפשו גנים שמתמחים בייצור סוגי תאים חדשים בזמן ההתפתחות העוברית. כל אחד מהם חקר גֵן אחר שהשפיע על התזמון של תהליכים התפתחותיים בתולעת. אמברוז התמקד בגֵן lin-4, והבחין שהוא גורם לירידה בביטוי של גֵן אחר, lin-14. אבל הוא לא הבין את המנגנון שעומד מאחורי זה. ההשערה ההגיונית ביותר מבחינתם הייתה ש-lin-4 אחראי ליצירת גורם שעתוק חלבוני שמדכא את הביטוי של lin-14, אבל הרצף של הגֵן lin-4 היה קצר מאוד, ולא היו לו המאפיינים הדרושים לייצור חלבון.
ממש באותה תקופה הקים רובקון מעבדה משלו בבית החולים הכללי של מסצ'וסטס, והמשיך לעסוק בשאלה שהטרידה אותו במהלך הפוסט-דוקטורט: מה המנגנון שמשתיק או מדכא את הגֵן lin-14. הוא ראה שבתאים בהם יש דיכוי של הגן, עדיין נוצר RNA שליח של lin-14, אבל נוצרים ממנו פחות חלבונים. זה נראה לו מוזר: החלבונים שמבקרים את ביטוי הגנים עושים זאת בשלב השעתוק, ומדכאים את יצירת ה-RNA שליח.
אם כך, אולי מדובר במנגנון דיכוי אחר, שמתרחש בשלב מאוחר יותר?
רובקון ואמברוז השוו את ממצאיהם, וגילו שהגנים שחקרו, lin-4 ו-lin-14, אחראים לייצור מולקולות RNA משלימות – כלומר בחלקים מסוימים הן יכולים להיצמד זו לזו. בניגוד ל-DNA, שבנוי כ"סליל כפול" ומורכב משני גדילים – שנצמדים זה לזה ומשלימים זה את זה, כמו שני הצדדים של רוכסן – מולקולת RNA בנויה כגדיל אחד בלבד. ה-RNA הקצר של lin-4 נצמד לקטע מסוים ב-RNA של lin-14, ליצירת מבנה דו-גדילי. המבנה הזה מונע מהריבוזום לקרוא את ה-RNA של lin-14 ולייצר חלבון על פיו, ועשוי גם לזרז את הפירוק של ה-RNA שליח.
כך גילו שני החוקרים סוג חדש של RNA – מיקרו-RNA, מולקולות קטנות שאינן מכילות הוראות לייצור חלבון, ותפקידן לווסת את ייצור החלבונים. בניגוד לגורמי השעתוק החלבוניים, מיקרו-RNA פועלים לאחר שה-RNA שליח של הגנים האחרים כבר יוצר, ומונעים ייצור החלבון על פיו. כך התא יכול לפעול במהירות, בשעת הצורך, ולעצור ייצור חלבונים שה-RNA שליח שלהם כבר שועתק – למשל האורגניזם אינו צריך לייצר חלבונים המגנים על ה-DNA מהתחממות, אם הטמפרטורה כבר ירדה. הם פרסמו את ממצאיהם בשני מאמרים צמודים, הראשון והשני ב-1993.
מנגנון שמור היטב
בהתחלה לא נרשמה התרגשות רבה בקהילה המדעית: רבים חשבו שהמנגנון החדש עשוי להיות ייחודי לתולעים שהם חקרו, ואינו רלוונטי לבעלי חיים אחרים. זה השתנה כאשר בשנת 2000 רובקון ועמיתיו גילו מיקרו RNA חדש, לו הם קראו let-7. הגן הזה כמעט ולא השתנה לאורך מיליוני שנות אבולוציה, ונמצא בגנום של בעלי חיים רבים, לא רק אצל הנמטודות.
זה כבר היה רמז לכך שמיקרו-RNA הוא מנגנון נפוץ, וחוקרים רבים החלו להתעניין במולקולות הקטנות. תוך שנים ספורות התגלו מאות גנים של מיקרו-RNA. כיום ידוע שהמנגנון הזה נמצא בכל היצורים הרב-תאיים, לא רק בעלי חיים אלא גם צמחים ופטריות, ונראה שהוא חיוני להתפתחותם. חוקרים מעריכים שלבני אדם יש יותר מאלף מיקרו-RNA שמסוגלים לדכא את הביטוי של אלפי גנים. היות שמולקולות מיקרו-RNA הן קטנות כל כך, בין 21 ל-23 בסיסים בלבד, מולקולה מסויימת יכולה לעתים קרובות להיצמד ל-RNA שליח של כמה גנים, כי אצל כולם יש את אותו רצף קצר שמתאים לרצף שלה.
חקר המיקרו-RNA לימד אותנו רבות על הדרך שבה התאים מבקרים את ייצור החלבונים שלהם. בנוסף, הוא מאפשר לנו לבדוק מה קורה כאשר המנגנון הזה אינו פועל כראוי. מחקרים מראים שביטוי לא תקין של מיקרו-RNA יכול לגרום למחלות רבות, ביניהם סרטן, בעיות במבנה השלד ובאיברים שונים, ועוד. ואם חוסר או עודף של מיקרו-RNA מוביל למחלות, ייתכן שאפשר יהיה לפתח טיפולים שיתבססו על אותן מולקולות קטנות.
על עבודתם המשותפת זכו רובקון ואמברוז בפרסים רבים, בהם מדליית בנג'מין פרנקלין ב-2008, פרס דן דוד, המוענק באוניברסיטת תל אביב, שאותו קיבל רובקון ב-2011 עם הביולוגית סינתיה קניון (Kenyon). ב-2014 רובקון ואמברוז זכו יחד בפרס וולף, עם החוקר הישראלי לשעבר נחום זוננברג, הנחשב למנבא מוצלח של זכיות בפרסי נובל בתחומים הרלוונטיים. כמו כן הם זכו בפרס Breakthrough היוקרתי ב-2015, ובפרס "מצעד הפרוטות" לביולוגיה התפתחותית ב-2016.
פרס נובל לפיזיולוגיה או לרפואה מוענק מדי שנה מאז 1901 על-ידי מכון קרולינסקה השבדי למי שתרמו תרומה ייחודית או ביצעו מחקר יוצא דופן בפיזיולוגיה או ברפואה. בשנה שעברה חלקו את הפרס פרופ' קתלין קריקו, ביוכימאית מהונגריה, ופרופ' דרו ווייסמן, אימונולוג יהודי-אמריקני, על תגליתם שהובילה לפיתוח חיסוני mRNA לקורונה של פייזר ומודרנה. הם גילו את השינויים ב-RNA, שנדרשים להפוך אותו למתאים לטיפול והניחו את היסודות לחיסוני ה-mRNA נגד קורונה.
כתבה זו הוכנה בסיוע ד"ר יונת אשחר, ד"ר מעיין קרלינסקי צור ונעם לויתן. למידע ולכתבות נוספות באתר מכון דוידסון לחינוך מדעי