ברמת דיוק שלא הייתה מביישת כלי טיס הנוחת על נושאת מטוסים, מצליחים תאי המערכת החיסונית לנוע בכלי הדם במהירות מסחררת, אך יודעים לבלום בעת הצורך. יכולת מופלאה זו מאפשרת להם לעצור בנקודה מדויקת על דופן כלי הדם כדי לחדור לרקמה פגועה או לקשרי הלימפה בגוף בחיפוש אחר סימני זיהום. כיצד מצליחים התאים לזהות את נקודות העצירה בדיוק כה יוצא דופן? מדעני מכון ויצמן למדע יצאו לחקור את הנושא ומצאו כי תאים חיסוניים חיוניים, הקרויים תאי T, מצוידים בציוד בלימה הנמצא, פשוטו כמשמעו, בקצות אצבעותיהם.
אנחנו נוטים לדמיין תאים ככדוריות חלקות, אך פני השטח של רבים מהם – ובוודאי של כל תאי המערכת החיסונית – אינם חלקים כלל. על הקרום החיצוני של התא ישנן בליטות גמישות הדומות לאצבעות זעירות, העוזרות להם לחוש את הסביבה ולתקשר איתה.
כדי לחצות את דופן כלי הדם ולחדור אל קשר הלימפה, "אצבעותיהם" של תאי המערכת החיסונית מסוג T נקשרות לחלבונים מיוחדים הנמצאים על הדופן. לאחר ההיקשרות, מתגלגלים התאים לאורך הדופן עד אשר קולטנים שלהם, בשם CCR7, נתקלים בכימוקינים של קשר הלימפה. מולקולות קטנות אלה מודיעות לתאי T: "ברוכים הבאים, הגעתם ליעד". משם עובר המסר הלאה בתוך התא ומפעיל את החלבון LFA-1 הנקשר למולקולות ספציפיות דביקות על דופן כלי הדם.
4 צפייה בגלריה


אצבעות על פני השטח של תא T. צולם באמצעות מיקרוסקופ אלקטרונים סורק
(צילום: מסע הקסם המדעי, מכון ויצמן למדע)
כך התא עוצר בחריקת בלמים, יוצא מכלי הדם וחודר לקשר הלימפה, שבו הוא מבצע סריקה הנמשכת בין דקות מספר לכמה שעות, ואם אינו מוצא גורם זר – חוזר למחזור הדם כלעומת שבא; אלפי סריקות כאלה מתבצעות בכל דקה במאות קשרי הלימפה בגוף כדי להבטיח את בריאותנו.
במחקר קודם גילו פרופ' רונן אלון וחברי קבוצתו במחלקה לאימונולוגיה כי אות הבלימה נוצר באצבעות תאי T בתוך פחות מחצי שנייה. מהירות זו מפתיעה במיוחד, שכן תא T מתגלגל בכל שנייה מרחק של כ-0.1 מילימטר, כלומר פי 15 לערך מקוטרו – קצב המקביל למהירות של מטוס קרב בשלבי הנחיתה. אך כאשר מטוס נוחת על מנחת צר, כבלי פלדה המיועדים לעצירתו כבר פרוסים ומוכנים לפעולה. לעומת זאת, כאשר תא T "נוחת", נראה שהוא צריך להרכיב את ציוד הנחיתה בקצות אצבעותיו בכל פעם מחדש. יתר על כן, בעבר התגלה כי החלבון LFA-1 – החיוני לבלימה – נמצא חבוי ברובו על גוף התא, הרחק מקצות האצבעות הזעירות המכסות את פני השטח שלו.
ציוד הבלימה נמצא בקצות האצבעות
כדי להבין כיצד מצליח תא T להרכיב את ציוד הבלימה שלו במהירות שיא, חבר פרופ' אלון לפרופ' גלעד הרן מהמחלקה לפיסיקה כימית וביולוגית, אשר פיתח גישה חדשה לחקר פני השטח של תאים ברמה של מולקולות בודדות באמצעות מיקרוסקופיה ברזולוציית-על. מדובר בשילוב בין שתי טכנולוגיות: שיטה אחת לקביעת מיקומן של מולקולות שונות באמצעות סמנים פלואורסצנטיים, ושיטה נוספת ליצירת מעין מפות טופוגרפיות של פני שטח התא, כולל אצבעותיו, על בסיס עוצמת האות הפלואורסצנטי. "אנחנו ממפים את הגבעות והעמקים על פני שטח התא ויוצרים מפה טופוגרפית הדומה לזו המציגה את צורת פני השטח של כדור-הארץ", מסביר פרופ' הרן.
4 צפייה בגלריה
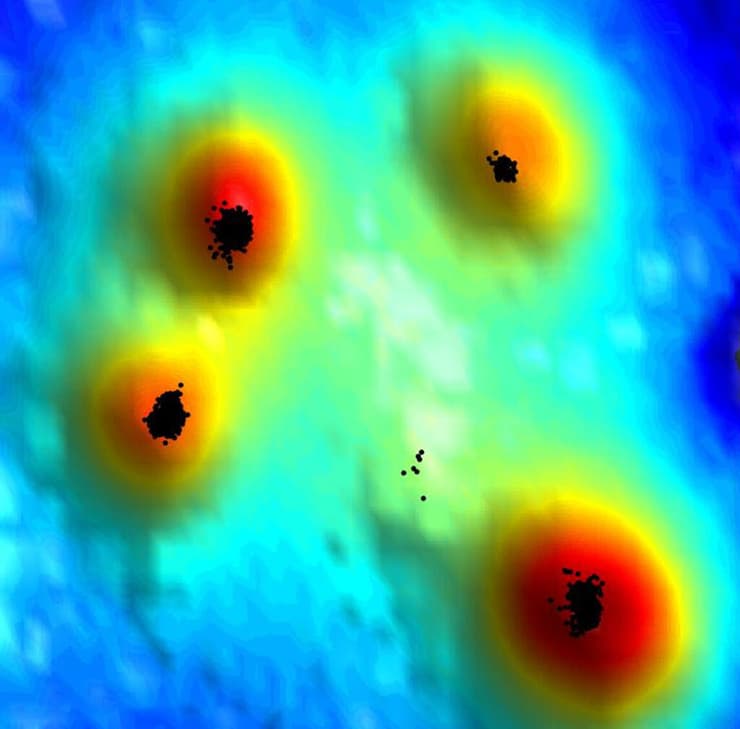

מפה טופוגרפית של מקטע על פני השטח של תא T. האזורים האדומים הם האצבעות הגמישות המתוארות במאמר (ככל שהצבע חם יותר, כך האזור המסומן גבוה יותר). קולטני CCR7 (בשחור) ממוקמים בנקודות הגבוהות ביותר על פני האצבעו
(צילום: מסע הקסם המדעי מכון ויצמן למדע)
ד"ר שירסנדו גוש, חוקר בתר-דוקטוריאלי במעבדתו של פרופ' הרן, וד"ר שרה פייגלסון ממעבדתו של פרופ' אלון, הובילו את המחקר החדש, שבמסגרתו גילו המדענים כיצד מבצעים תאי T את פעלול הבלימה שלהם.
כל הציוד הדרוש לבלימה מהירה מוכן להרכבה בקצות האצבעות של תאי T. כך יכולים התאים לייצר את אות הבלימה בתוך פחות מחצי שנייה
הם מצאו כי קולטני CCR7 מרוכזים בחלק הנגיש ביותר – בדיוק בקצות האצבעות של התאים. כמו כן, התגלה כי מולקולות ה-LFA-1 נמצאות אמנם ברובן על גוף התא, אך כ-5% מהן נמצאות על פני האצבעות בקרבת CCR7. דבר נוסף ולא פחות חשוב: כל מולקולות העזר הדרושות להעברת אותות הבלימה נמצאו גם הן בקצות האצבעות, בסמיכות לקולטני CCR7. "כל הציוד הדרוש לבלימה מהירה מוכן להרכבה בקצות האצבעות של תאי T. כך יכולים התאים לייצר את אות הבלימה בתוך פחות מחצי שנייה", אומר פרופ' אלון.
לבד מחשיפת דרכי הפעולה של המערכת החיסונית, ממצאי המחקר פותחים את הדלת גם בפני חקר המנגנונים השולטים בתנועת תאים שונים, ובהם תאי סרטן העלולים להיסחף במחזור הדם ולעצור במקומות שונים לצורך יצירת גרורות.
הממצאים עשויים גם לעזור לפתח דרכים לשלוט בתנועתם של תאי המערכת החיסונית: כך ניתן יהיה, למשל, להגדיל בהנדסה גנטית את מספר קולטני CCR7 באצבעות התאים כדי לזרז את הגעתם לקשרי הלימפה ולהגביר בכך את יעילותם של חיסונים שונים, או, לחלופין, לרסן את תנועתם של תאי חיסון מזיקים הפועלים במחלות אוטואימוניות.
4 צפייה בגלריה


מימין לשמאל: ד"ר שירשנדו גוש, פרופ' רונן אלון, פרופ' גלעד הרן וד"ר שרה פייגלסון. בקצות האצבעות
(צילום: מסע הקסם המדעי, מכון ויצמן למדע)
במחקר השתתפו ד"ר אלסיו מונטרסור ופרופ' קרלו לאודנה מאוניברסיטת ורונה שבאיטליה; ד"ר אייל שמעוני מהמחלקה לתשתיות למחקר כימי במכון ויצמן למדע; ד"ר פרנססקו רונקטו מהמחלקה לאימונולוגיה של המכון ופרופ' דניאל לגלר ממכון הביוטכנולוגיה תורגאו, שווייץ, השייך לאוניברסיטת קונסטנץ.







