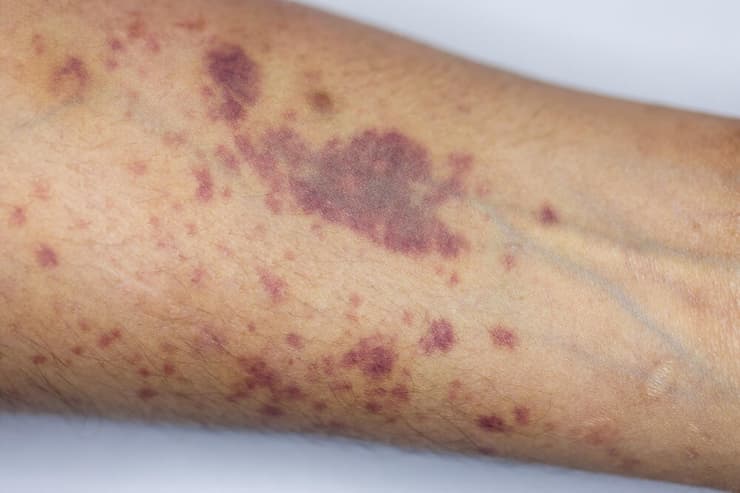
המופיליה, המחלה שעומדת במוקד פרשת הביציות שיובאו מגאורגיה לישראל, מתבטאת בדימומים פנימיים או חיצוניים, שעלולים אפילו לסכן חיים. דימומים אלה יכולים להיגרם עקב חבלות ופגיעות, אך גם באופן ספונטני. המחלה התורשתית שנגרמת כתוצאה מפגם בכרומוזום X, תקפה לאורך ההיסטוריה שושלות מלוכה באירופה והיא פוגעת בעיקר בזכרים, צאצאים לנשים שנושאות את הגן הפגום.
ד"ר מוטי חיימי, מומחה ברפואת ילדים והמטולוגיה ילדים במאוחדת ורופא מרחב חוף כרמל ואדי ערה במחוז צפון של מאוחדת, מספק רקע על ההיסטוריה של המחלה: "היא מאובחנת בעיקר בילדים ונזכרה לראשונה בתלמוד, כשבעיר ציפורי אישה ילדה שני בנים שדיממו למוות אחרי ברית המילה. חכמי התלמוד הורו שלא למול את הילד השלישי של אותה אישה, כי הם הבינו שיש מחלה תורשתית של הבנים הזכרים.
 ד"ר מוטי חיימיצילום: דוברות מאוחדת
ד"ר מוטי חיימיצילום: דוברות מאוחדת"המופיליה הייתה גם נפוצה מאוד בקרב בתי המלוכה באירופה. המלכה ויקטוריה מאנגליה הייתה נשאית והיא העבירה את זה לצאצאים שלה בדורות הבאים. אחד מהם, הנסיך לאופולד, מת בגיל 30 בגלל דימום מוחי. יש שמשערים שהמחלה הזו מהווה את אחד המקורות למונח 'דם כחול', כי אחד מסממני המחלה הוא דימום שגורם לעור להיות בגוון כחלחל". נזכיר שלא רק באנגליה, המחלה עברה גם לצאצאים בבתי המלוכה ברוסיה, פרוסיה וספרד.
קיימים שני סוגי המופיליה: A ו-B. בסוג האחד יש חסר של פקטור 8 ובאחר חסר של פקטור 9. המופיליה A שכיחה יותר - אחת ל-5,000 לידות זכרים. המופיליה B (זו מפרשת הביציות) מופיעה בשכיחות של אחת ל-30-20 אלף לידות זכרים. שני סוגי המחלה באים לידי ביטוי באופן דומה: הפרעה שגורמת לדימומים בכל מיני מקומות בגוף, בחלק מהמקרים עד כדי סכנת חיים.
ממה בדיוק נגרמת מחלת ההמופיליה?
ד"ר קארין ויס, מנהלת המכון הגנטי במרכז הרפואי רמב"ם: "יש לנו כמה פקטורי קרישה בגוף שאחראים על תהליך הקרישה של הדם. במחלה הזאת נפגע פקטור 9. מדובר במחלה גנטית שפוגעת בגן שקשור לכרומוזום ה-X והיא מתבטאת בעיקר אצל זכרים ופחות בנקבות, מכיוון שבנקבות יש שני עותקים של כרומוזום X ואצל זכרים יש X ו-Y, אז אין כרומוזום נוסף שמפצה. לכן, יכול להיות מצב של אישה נשאית של מוטציה בגן שהיא בריאה לחלוטין, לא יודעת מזה ויכולה להעביר את המחלה לבנים שלה".
 ד"ר קארין ויסצילום: הקריה הרפואית רמב"ם
ד"ר קארין ויסצילום: הקריה הרפואית רמב"םפרופ' סתוית אלון-שלו, מנהלת המכון לגנטיקה במרכז הרפואי העמק מקבוצת כללית, מוסיפה: "המופיליה B היא מחלה שקשורה בפגיעה במערכת קרישת הדם. היא נובעת מחסר של מרכיב חשוב, חלבון שנקרא פקטור 9 שהוא הכרחי לתהליך הקרישה המורכב שיש לכל אדם בריא. רוב הגנים שמופיעים על כרומוזום X לא קיימים על כרומוזום Y והמשמעות היא, שאצל זכר בעל מוטציה בגן שממוקם על כרומוזום X המחלה תתבטא באופן חמור".

איך מתבטאת הבעיה במנגנון הקרישה של חולי המופיליה?
ד"ר דועאא עכאשה, המטולוגית במרכז הרפואי העמק מקבוצת כללית, אומרת כי "ברגע שאנחנו נפצעים, מערכת הקרישה מופעלת על מנת לעצור את הדימום בעזרת שני תהליכים עיקריים: תהליך קרישה ראשוני שהוא 'העזרה הראשונה' שמגיעה לאזור הפצוע ומבוססת על שפעול טסיות הדם, ותהליך קרישה שניוני שבו נכנסים לפעולה רוב פקטורי הקרישה, שאחד מהם הוא אותו פקטור 9. כשיש פגיעה במערכת הראשונית, זה בא לידי ביטוי בדימומים מידיים ושטחיים ודימומים מריריות. כשיש פגם במערכת הקרישה השניונית, זה יבוא לידי ביטוי בדימומים עמוקים - בחללים, בשרירים, בפרקים, בדימום תוך מוחי וברטרופריטונאום (אזור בבטן)".
מה השכיחות של מחלת ההמופיליה?
ד"ר דוד איסקוב, מומחה פוריות, מנהל מרכז בריאות האישה במרכז רפואי זבולון של כללית, מחוז חיפה וגליל מערבי, אומר כי אחד מסוגי ההמופיליה שכיח יותר והאחר פחות. "בסוג A, שבו חסר פקטור 8, השכיחות היא 1 ל-5,000 זכרים. השכיחות של המופיליה B, שבה יש חסר של פקטור קרישה 9, היא 1 ל-30,000. פקטורי הקרישה הם חלבונים שמופעלים יחד במטרה לעצור את הדם בזרימתו ולהפוך אותו מנוזל למוצק בעזרת חומר שנוצר שנקרא פרותרומבין וכך בסופו של דבר נוצרת קרישה. ברגע שחסר אחד החלבונים האלו, יש סיכוי גבוה יותר לדמם והמחלה גורמת למעשה לדימומים מכל דבר קטן".
 פרופ' סתוית אלון-שלוצילום: דוברות המרכז הרפואי העמק
פרופ' סתוית אלון-שלוצילום: דוברות המרכז הרפואי העמקד"ר סתוית אלון-שלו מהעמק, מציינת כי מידת השכיחות של נשים בעלות מוטציה בגן הקשור להמופיליה B, כמו במקרה שתואר בפרשת הביציות החדשה, היא נמוכה יחסית. המחלה נדירה ולכן היא לא עומדת בקריטריונים של סקר גנטי לאוכלוסייה הכללית. "בודקים אותה רק אם עולה חשד או אם ידוע על חולים במשפחה. אישה שהיא נשאית של מוטציה בגן להמופיליה B היא בסיכון של 50% להעביר אותו לכל אחד מצאצאיה: אם הצאצא ממין נקבה, הביטוי הרפואי צפוי להיות קל או שלא יהיה כלל. אם צאצא ממין זכר יקבל את המוטציה, הוא צפוי להיות פגוע במחלה חמורה. במילים אחרות: 50% מהבנים של אישה נשאית צפויים להיות פגועים במחלה באופן קשה".
ד"ר קארין ויס מרמב"ם מציינת שבגלל היעדרן של בדיקות גנטיות לכל האוכלוסייה, "יכול מאוד להיות שתהיה תורמת ביצית נשאית שלא ידעה, כי היא עצמה בריאה".
מדוע המחלה כה מסוכנת?
המופיליה מתבטאת בדימומים חוזרים באיברים הפנימיים, בעיקר במפרקים, שעלולים לגרום להרס המפרקים ולנכות קשה. ד"ר חיימי ממאוחדת מסביר: "הביטויים של שני סוגי ההמופיליה (A ו-B) דומים - הפרעה גנטית שגורמת לדימומים בכל מיני מקומות בגוף. הדימום יכול להיות בעור או דימומים לתוך השרירים. הרבה פעמים רואים את זה על תינוקות אחרי חיסון או בזמן בקיעת שיניים, ברית מילה או דימום בגולגולת בזמן הלידה. ייתכן אפילו דימום מוח במקרים חמורים. המחלה עלולה לגרום לנכות בגלל דימום חוזר במפרק, הוא נפגע וצריך לעשות ניתוחים להחלפת מפרקים".
"חומרת המחלה", מסביר ד"ר חיימי, "תלויה ברמת החסר של הפקטור. בחוסר קל, יכול להיות שהדימום לא יהיה ספונטני, אלא יתבטא רק בזמן ניתוח או חבלה, אבל בחסר קשה יכול להופיע דימום באופן ספונטני ואפשר לאבד הרבה דם, אפילו ליטר של דם מדימום במפרק. יש פגיעה באיכות החיים בעיקר בגלל דימומים חוזרים במפרקים שגורמים להרס ולעיוות שלהם. אותם ילדים עלולים להישאר נכים, צולעים ועוברים הרבה ניתוחים וכאבים".
 ד"ר דועאא עכאשהצילום: דוברות המרכז הרפואי העמק
ד"ר דועאא עכאשהצילום: דוברות המרכז הרפואי העמקד"ר עכאשה מהעמק, מוסיפה: "כשמדברים על המופיליה B, היא מסוכנת כי יש לחולים יותר נטייה לדימומים ספונטניים או לחבלות מינוריות. חולי המופיליה יכולים לסבול מדימום פנימי עמוק - דימום בבטן, בשרירים ובמפרקים כמו בברך, בירך ובמרפק. זה עלול להפעיל לחץ על המפרקים ולגרום לכאבי מפרקים. אם זה נמשך זמן רב וללא טיפול, ייתכן שתתפתח במקום דלקת מפרקים והמצב עלול להידרדר עד להרס של המפרק, איבוד טווחי תנועה ונכות משמעותית".
איך מאבחנים את המחלה?
ד"ר ויס מרמב"ם מזכירה שהבדיקה נעשית רק כשיש חשד למחלה, "זה לא משהו שבהכרח אפשר לדעת. כשיש תורמת, צריך לשאול אם יש מחלות במשפחה ואם יש היסטוריה. צריכים לעשות בדיקות בהתאם. המופיליה לא נמצאת ברשימת הבדיקות בסקר הגנטי".
ד"ר עכאשה מהעמק מוסיפה ש"המחלה מאובחנת באמצעות בדיקת דם, שם בודקים את כמות פקטור הקרישה בדם. ניתן לזהות רמז לחסר זה באמצעות בדיקת תפקודי קרישה כשרואים הארכה של ערך שנקרא aPTT. בדיקה זו בוחנת כמה זמן לוקח לדם להתקרש".
ד"ר חיימי: "כשרואים שמשך ה-PPT מתארך, ממשיכים לבדוק את הפקטורים 8 ו-9 שיכולים לגרום למחלה. בודקים את הפעילות והרמה שלהם. לפי זה יודעים את רמת הפקטור - קל, בינוני או קשה".
ד"ר דוד איסקוב: "צריך לחנך את הציבור לדרוש, לבקש ולהיענות לעשות כמה שיותר בדיקות גנטיות ולא לחכות עם זה. כיום יש אפשרות לבדוק 200 גנים לפחות לעומת חמישה שמשרד הבריאות המליץ בזמנו. מומלץ לעשות פאנל גנטי מורחב שנותן לזוג הרבה יותר שקט"
מה עושים לקראת היריון? איך נדע שלא קיבלנו תרומת ביצית מאישה נשאית המופיליה?
פרופ' אלון-שלו אומרת שכאשר אישה מתכננת היריון, או מיועדת לתרום ביציות, יש לברר אם קיימות מחלות רקע אצלה, או מחלות במשפחה, או כל נתון רפואי שיכול להיות קשור בסיכון יתר לצאצאים ולבצע בדיקות בהתאם לנתונים. "צריך לוודא שהיא מבצעת בדיקות גנטיות של מצבים שכיחים יחסית לפי המוצא האתני שלה. אם קיים סיכון למחלה במשפחה, הדרך הנכונה היא הפניה לייעוץ גנטי, ששם ישוחחו על הסיכונים לפי עץ המשפחה ועל הבדיקות העומדות לרשות הנבדקים.
"אם ידוע שאישה נשאית מוטציה בגן המקודד את פקטור 9 והאישה מעוניינת בתכנון משפחה כך שלא ייוולדו לה בנים פגועים, ניתן להציע לה אבחון טרום לידתי או אבחון טרום השרשה. אבחון טרום לידתי מבוצע בהיריון - באמצעות ביופסיה מסיסי שליה או באמצעות דיקור מי שפיר. אבחון טרום השרשה מצריך הפריית מבחנה, שבמהלכה מבצעים בדיקה גנטית בתא שנלקח מביצית מופרית. בהמשך מחזירים לרחם האם עוברים שנבדקו ואינם פגועים במחלה".
ד"ר איסקוב מוסיף שכאשר אישה באה לייעוץ לפני היריון, מומלץ לה לעשות כמה שיותר בדיקות גנטיות. בהקשר זה, אומר ד"ר איסקוב: "צריך לחנך את הציבור לדרוש, לבקש ולהיענות לעשות כמה שיותר בדיקות גנטיות ולא לחכות עם זה. המלצות משרד הבריאות עד היום הן סקר גנטי של חמש מחלות גנטיות בסיסיות השכיחות ביותר בקרב האוכלוסייה. בעקבות השינוי בסל השירותים של משרד הבריאות יש אפשרות לאסוף מידע גנטי נרחב יותר. במקביל אנחנו ממליצים להיפגש עם יועץ גנטי שייתן שקט לזוג.
 ד"ר דוד איסקובצילום: דוברות כללית
ד"ר דוד איסקובצילום: דוברות כללית"כיום יש אפשרות לבדוק 200 גנים לפחות לעומת חמישה שמשרד הבריאות המליץ בזמנו. מומלץ לעשות פאנל גנטי מורחב שנותן לזוג הרבה יותר שקט. אנחנו ממליצים על ייעוץ גנטי לפי המוצא של הזוג. כשמדובר בטיפול הפריה חוץ-גופית על אחת כמה וכמה אנחנו דורשים שיהיו בדיקות גנטיות לשני בני הזוג. אנחנו תמיד צריכים להמליץ ולהסביר את המשמעויות וכל זוג בוחר מה לעשות עם זה".
"בנושא של תרומת ביצית הסיפור שונה", מסביר ד"ר איסקוב, "כי התורמת לא בידיים שלנו. אנחנו הרופאים של הזוג שנמצא בארץ. לאישה אין אפשרות להשתמש בביציות שלה ואנחנו נזקקים לתרומות. מספר התרומות בארץ קטן ולכן הרבה תרומות ביציות מגיעות מחו"ל. ואז קורה תהליך שבו הזרע של הבעל עובר הקפאה ומוטס לעשות הפריה לביציות של תורמת צעירה, בדרך כלל מארצות מזרח אירופה. לכן רצוי להמליץ לבעל שיעשה כמה שיותר בדיקות גנטיות, לעשות לו פאנל גנטי מורחב. המידע שאנחנו מקבלים על התורמת הוא על-פי הוראות משרד הבריאות לחמש מחלות מאוד בסיסיות. כמובן שהרופא המטפל בחו"ל צריך לוודא התאמה בין התורמת לבן זוג הנתרמת".
ד"ר מוטי חיימי: "הטיפולים כיום שיפרו מאוד את תוחלת החיים של חולי המופיליה, ועדיין יש סכנות וצריך להיזהר ולהישמר בטיפולי שיניים, בניתוחים ובכלל. למרות שהמחלה גורמת לפחות תמותה מבעבר, היא עדיין עלולה להיות מסוכנת במצבים מסוימים. אפשר ועדיף למנוע אותה"
איך מטפלים בהמופיליה B?
ד"ר עכאשה מהעמק: "הדרך הטובה ביותר לטפל בהמופיליה היא על ידי מתן תחליף לפקטור הקרישה החסר כדי שהדם יוכל להיקרש כראוי. זה נעשה בדרך כלל על-ידי מתן מוצר דם שנקרא פלזמה שמכיל ריכוז גבוה של הפקטור החסר, או מתן תחליף רקומביננטי (שנוצר במעבדה) שאינו מגיע מפלזמה אנושית. ניתן לתת טיפול מיידי או טיפול מונע. טיפול מיידי משמש לעצירת דימום חריף. טיפול מניעתי משמש למניעת התרחשות של דימום".
ד"ר חיימי אומר כי הטיפולים כיום שיפרו מאוד את תוחלת החיים של חולי המופיליה, "שנעשתה כמעט רגילה. בעבר היו מחזירים לילדים החולים את הפקטורים החסרים ממנות דם של אנשים אחרים ואז הבעיה הייתה שהרבה חולי המופיליה נדבקו ב-HIV וגם בצהבות (הפטיטיס B ו-C) ולאחרונה במחלות ובווירוסים אחרים שמועברים בדם. בשנים האחרונות פיתחו תרופות מטוהרות שהן ממש הפקטורים עצמם שמונפקים מהדם ועוברים טיהור מזיהומים.
4 צפייה בגלריה

הפריה חוץ-גופית מאפשרת לבחון האם העוברים נושאים את המחלה לפני שיוחזרו לגוף האישה
(צילום: shutterstock)
"בנוסף, התחילו לתת פקטור 7 משופעל שבעצם עוקף את פקטור 8 ו-9 (הפגומים) ומונע דימומים. כמו כן, ניתן לבצע ריפוי גנטי - להשתיל את הגן הבריא לילדים חולים אבל זה כבר הליך יותר מסובך. עדיין יש סכנות וצריך להיזהר ולהישמר בטיפולי שיניים, בניתוחים ובכלל לא לקבל חבלת ראש כי החולה יכול לדמם תוך דקות ולסבול מדימום מוחי. למרות שהמחלה גורמת לפחות תמותה מבעבר, היא עדיין עלולה להיות מסוכנת במצבים מסוימים. אפשר ועדיף למנוע אותה".
ד"ר ויס מוסיפה שהמופיליה היא מחלה כרונית שדורשת טיפול במשך כל החיים, ולכן היא פוגעת באיכות החיים, "זה תחום שמשתפר מבחינת טיפול. לאחרונה אושר בארה"ב טיפול גנטי בהמופיליה A שבו נותנים את הגן החסר כטיפול אבל זה לא הגיע לארץ עדיין, עניין של סל הבריאות. עולם הטיפול הגנטי מתפתח מאוד אבל הוא מאוד יקר ועוד לא ידוע מה יהיה מהבחינה הזאת בארץ".
בישראל חיים כ-800 חולי המופיליה מכל קצות החברה. הטיפול במחלה השתפר בצורה משמעותית בשנים האחרונות. רוב החולים מטופלים בטיפול מונע ומקבלים ליווי וטיפול רפואי שמאפשר להם לחיות חיים מלאים ופעילים, לעשות ספורט, להתנדב בצבא לטייל בחו"ל. הם מקימים משפחות ומפתחים קריירה. מעמותת על"ה נמסר שהיא "תומכת ומלווה את חולי ההמופיליה ומשפחותיהם בכל תחומי החיים וההתמודדות עם המחלה, אנחנו מזמינים כל משפחה שנפגעה בפרשה הזו לפנות אלינו".
בהכנת הכתבה השתתף אדיר ינקו