כבר לא מדע בדיוני
כשפורסמה לראשונה הטכנולוגיה, הרימו רבים גבה. האפשרות להוציא תאים מגופו של אדם, להנדס ולהרבות אותם, ואז להחזיר לגוף כדי להילחם בגידולים - נשמעה דמיונית. כשהתקבלו התוצאות הראשונות, שפשפו הרופאים את עיניהם בתדהמה: חולים שכבר אפסו הסיכויים להציל את חייהם, נוקו לחלוטין מסרטן. כעת הוכתרה CAR-T המהפכנית כטכנולוגיה פורצת דרך
בשיתוף סורוקה, מרכז רפואי אוניברסיטאי מקבוצת כללית
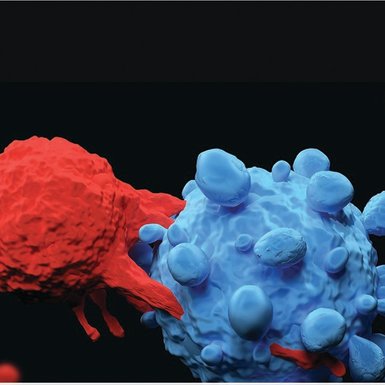
הטיפול הזה נשמע כל־כך עתידני, שרבים מהקהילה הרפואית הרימו גבה כשהוצג לראשונה. ואז הם ראו את התוצאות. הכירו את טכנולגיית CAR, במסגרתה לוקחים מחולים מנת דם, מוציאים ממנה את תאי הדם הלבנים מסוג T, ושולחים אותם למעבדה בארצות־הברית או אירופה. שם, בתהליך סודי ומורכב, מהונדסים התאים גנטית ומתווספים להם קולטנים (רצפטורים) מיוחדים שיודעים לזהות את הגידולים הסרטניים, לתקוף אותם ולמעשה לשחרר את הגוף מהגידולים. מנת הדם ה"מחומשת" נשלחת בחזרה לחולה ומוזרקת לגופו. סוף טיפול.
בכנס הסרטן השנתי בשיקגו (ASCO) של האיגוד האמריקאי לאונקולוגיה, הוצגו נתונים חדשים לגבי הטיפול החדשני מסוג car-t-cells, שכיום מתבצע בחולי לוקמיה לימפובלסטית חריפה (ALL), הנפוצה יותר בקרב ילדים וצעירים מתחת לגיל 25 ובקרב חולי לימפומה מסוגDLBCL האופיינית יותר למבוגרים. טכנולוגיות דומות, שפועלות על סוגים אחרים של תאים, כבר נכנסו אף הן לשימוש ונמצאות במחקרים שונים ברחבי העולם. בכנס הסרטן השנתי, הוכתרה הטכנולוגיה כפורצת דרך.
רגע לפני הסוף
"על פני הגידולים ישנו חלבון שנקרא אנטיגן, שאינו ספציפי לגידול", מסביר פרופ' ארנון נגלר, מנהל המערך ההמטואונקולגי מהמרכז הרפואי שיבא בתל השומר. "מערכת החיסון מורכבת מחלק סלולרי – תאי T-cells, וחלק הומורלי, של הנוגדנים. במסגרת הטיפול המהפכני, מרכיבים את החלק של הנוגדן על פני תאי ה-T. בשפה הרפואית, זה נקרא כלאיים בין האנטיגן לבין הרצפטור על פני תאי ה-T".
החלבון הראשון שנגדו פותח ה-car-t, נקרא CD19, שמצוי בתאים סרטניים רבים. כאשר התאים המשודרגים מזהים את החלבון על התא, הם תוקפים אותו ומעלימים אותו מהגוף. בתחילה פורסמו תוצאות הטיפול על שני חולים, ואלה יצרו ציפיות חסרות תקדים ברחבי העולם מכיוון שללא הטיפול שני החולים לא היו כיום בין החיים. בהמשך, טופלו באותה שיטה חולים בלוקמיה חריפה, מחלה שכיחה בעיקר בילדים, ואחר כך גם בלימפומות – מחלה שכיחה יותר במבוגרים. "התוצאות היו מצוינות", אומר פרופ' נגלר, "ומדובר באנשים שכל הטיפולים האחרים נכשלו אצלם".
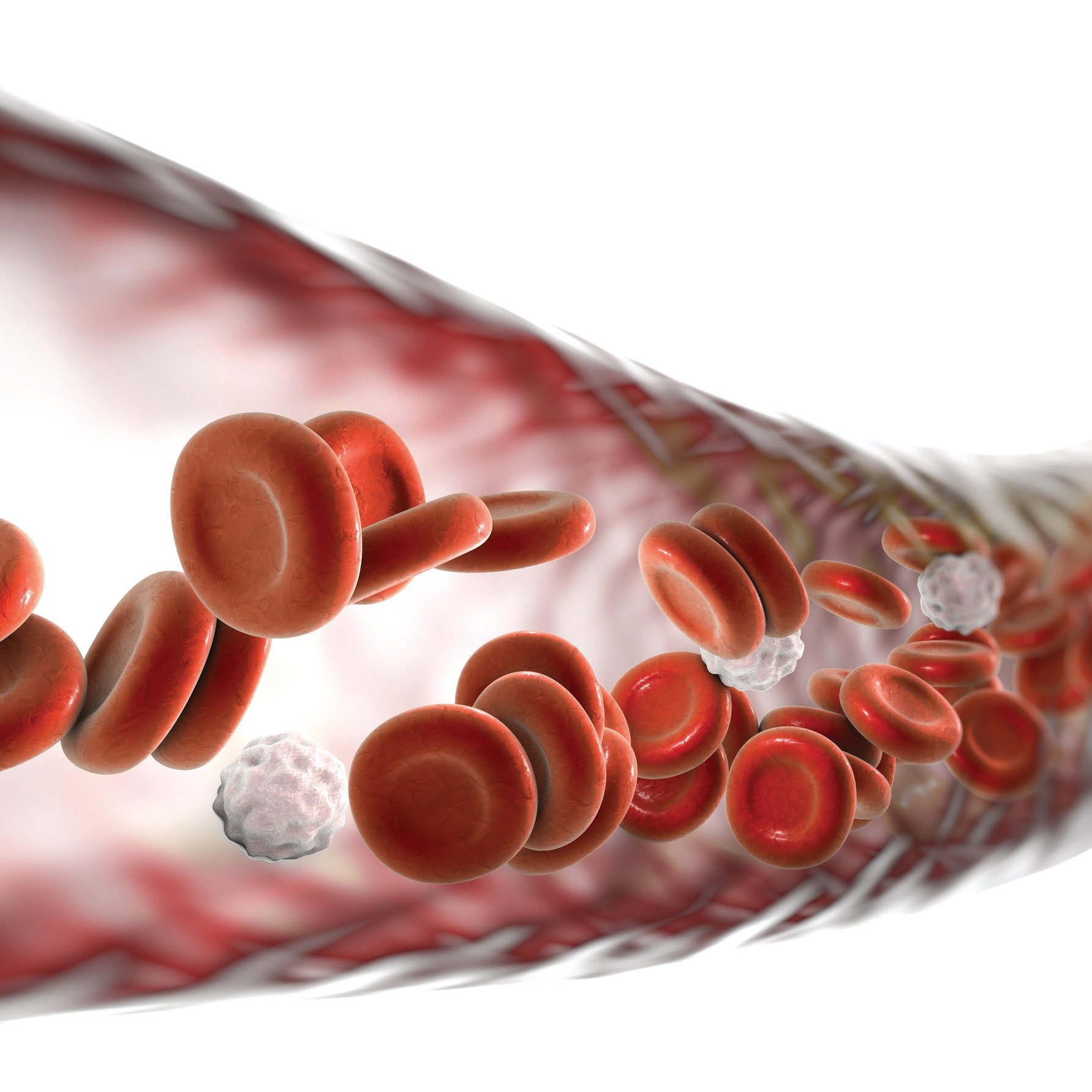
ALL היא מחלה של לימפוציטים (תאי דם לבנים) צעירים, בשלב שבו הם אינם בשלים עדיין, וקרויים לימפובלסטים או תאים בלסטים. במצב רגיל, תאי דם לבנים מתרבים בצורה מאורגנת ומבוקרת. בלוקמיה, לעומת זאת, התהליך יוצא מכלל שליטה והתאים מתרבים ללא בקרה, מבלי שהבשילו. תאים צעירים אלו ממלאים את מח העצם, ומונעים את ייצור תאי הדם התקינים.
DLBCL היא תת הסוג הנפוץ ביותר של Non Hodgkin Lymphoma. בלימפומה תאי מערכת החיסון מסוג לימפוציטים מתרבים ללא בקרה ופוגעים בלימופציטים התקינים, דבר הפוגע במערכת החיסון של הגוף.
"מדובר בחולים, שלרופאים כבר אין מה לעשות איתם", אומר פסקל טוסון, מנהל תחום טיפולי התא והגנטיקה בחברת התרופות נוברטיס, שלה הסכם עם בית הספר לרפואה באוניברסיטת פנסילבניה, שם פותחה בשנים האחרונות שיטת הטיפול.
"היחודיות של השיטה הזו", מוסיף טוסון, "הוא שלא מדובר כאן בתרופה שהרופא רושם ואוספים מבית המרקחת. זוהי טכנולוגיה מותאמת אישית. ההתאמה מבוצעת לכל חולה בנפרד. מכאן גם המורכבות של השיטה".
המחקר שהוצג בכנס הוא למעשה המשך מחקר קודם, שתוצאותיו הראשוניות הוצגו לפני זמן מה. "בהמשך המחקר רצינו לראות שמה שהתגלה בחודשי המחקר הראשונים (כעבור שלושה חודשים ושישה חודשים), אחוזים גבוהים מאוד של הפוגה מהמחלה, עדיין תקף".
ואכן, תוצאות המחקר מרשימות. אחרי 14 חודשים מהטיפול, כ-40% מחולי הלימפומה הראו הפוגה מוחלטת ו-12% נוספים הראו הפוגה חלקית. כלומר - 52% מהחולים הראו הפוגה כזו או אחרת מהמחלה, שהמשיכה להתקיים גם כעבור 12 חודשים עבור מרביתם.
מחקר נוסף שפורסם בכתב העת הרפואי New England of Medicine בחן את יעילות הטיפול בקרב חולי ALL צעירים והציג תוצאות מרשימות – 82% מהחולים הגיבו לטיפול והראו הפוגה מוחלטת מהמחלה שהמשיכה להתקיים גם כעבור 13 חודשים.
"זו רק ההתחלה", אומר עמנואל אוסטני, מנהל אזור אירופה של תחום טיפולי התא והגנטיקה בנוברטיס. "ככל שהזמן יעבור, מעריכים, זמן ההפוגה רק ילך ויגדל. ואל תשכח שמדובר כאן בחולים שלרפואה לא היתה עבורם תשובה. תאר לך מה יקרה אם ניתן את זה לאנשים במצב טוב יותר".
למעשה, קיימים כבר מקרים של חולים שלא נכללו במחקר, אך טופלו בשיטה וחיים כבר זמן רב. המטופל הרשום הראשון היה איש כוחות הביטחון, שתאי הלוקמיה כבר התפשטו בכל גופו. באוגוסט 2010 הוא קיבל מאות מיליוני תאי T של עצמו. כעבור ימים אחדים עלה חום גופו, לחץ הדם שלו ירד והוא סבל מקשיי נשימה, תופעות לוואי קשות שהביאו לאשפוזו בטיפול נמרץ. הסיבה לתופעות הלוואי: מערכת החיסון שלו הופעלה במידה מוקצנת בתגובה לתאים.
החולה התאושש, וכעבור חודש בלבד כבר לא מצאו הרופאים בבדיקות שלו שום סימן לנוכחות תאים סרטניים. התוצאות היו כל כך מדהימות, שהרופאים חזרו על הבדיקה וקיבלו תוצאות דומות.
חולה נוספת שטופלה עוד בראשית הדרך היא ילדה בת 6 עם לוקמיה שגססה מהמחלה והרופאים לא הותירו לה סיכוי לחיות. היא עברה את הטיפול וחיה עד היום – שש שנים לאחר שכבר חרצו את דינה. חולה אחר שטופל בטכנולוגיה, הגיע לטיפול לאחר שמצבו החמיר ולא נותרו לו אפשרויות טיפוליות אחרות, והוא חי עד היום ללא המחלה, כבר 29 חודשים.
במאמר שפרסמו החוקרים, הם הסבירו שכל תא T שהוחדר לגוף החולה, היה אחראי להמתה של עשרות אלפי תאים סרטניים. אותם תאים שהוחדרו לגוף החולים, המשיכו לעבוד גם כשהסרטן מוגר והראו יכולת לתקוף אותו אם ישוב.
צבא של מאות מיליונים
איך זה בעצם עובד? מדובר בתהליך שנמשך שלושה שבועות. לאחר שדגימה של תאי ה-T מוצאים מגופו של המטופל, הם נשלחים למעבדה בארצות-הברית או באירופה, שם מוסיפים להם את המרכיבים שמאוחר יותר ילחמו בתאים הסרטניים בגופו של החולה.
נוסף על כך, מכפילים את תאי ה-T של החולה, כך שבסופו של דבר יוזרקו מאות מיליוני תאים, שמתוכנתים לא רק להילחם בתאי הסרטן באופן מיידי – אלא גם להישאר בגוף לאורך זמן רב, ואם צריך אף להכפיל את עצמם בעתיד אם הגוף יפתח תאים סרטניים חדשים שצריך להילחם בהם. כלומר פעולה מיידית ופעולה משמרת לתקופה ארוכה יותר. לאחר הזרקת הדם מחדש בגופו של החולה, נדרשת תקופה של אשפוז בבית החולים, כדי לעקוב אחרי תופעות לוואי אפשריות ולטפל בהן.
לאחר תוצאות המחקרים הראשוניים בטכנולוגיה, החליטו ב־FDA להעניק לשיטה מעמד של טיפול פורץ דרך. למעשה, אישור השיווק ניתן תוך חמש שנים בלבד, לעומת זמן כפול בדרך כלל לתרופות אחרות. "תקופת ההישרדות הממוצעת של חולים אלה עומדת על שישה חודשים ללא הטיפול, כלומר עם הטיפול הסטנדרטי המקובל", מסביר אוסטני, "לכן הצורך בטיפול אפקטיבי יותר היה גבוה מאוד, וזו הסיבה שהאישור ניתן במהירות יחסית".
בישראל ישנם כ-100 חולים שיכולים ליהנות מהטיפול, וכיום נבדקת האפשרות לטפל בטכנולוגיה גם בחולים בשלבים מוקדמים יותר של המחלה. כלומר, לא רק במקרים שבהם כבר לא נותרה כל ברירה אחרת. הנושא נמצא כיום במחקרים, שתוצאותיהם יפורסמו בעתיד.
כמו בכל טיפול לסרטן, גם לזה ישנן תופעות לוואי שונות כמו חום, לחץ דם נמוך, קשיי נשימה ולעיתים גם תופעות של רעילות מהתאים המוחדרים לגוף. "מדובר בתופעות לוואי זניחות כי בקרב כל המטופלים שלנו איכות החיים השתנתה לחלוטין", הסביר אוסטני. "במקום לעבור טיפולי כימותרפיה חוזרים ונשנים בבתי החולים במשך תקופות לא קצרות, הם מקבלים טיפול אחד, וגם אם יש מעט תופעות לוואי, לא צריך לחזור עליו והם חוזרים לחיות חיים נורמליים".
לאחרונה פורסם סיפורו של אמיר, בן 44 ממרכז הארץ, שאובחן עם לימפומה ולא הגיב לטיפולים המקובלים. "סבלתי מכאבים בזמן ריצה והתלוננתי עליהם", הוא סיפר. "בתחילה שויכו הכאבים לבעיה אורטופדית, ולאחר בדיקות מקיפות נמצא בבדיקת סי.טי מעין 'חור' בעצם האגן . בהמשך התברר שזו לימפומה אגרסיבית, בדרגה 4, מפושטת באזורים רבים בגוף".
אמיר הספיק לעבור שני מחזורי כימותרפיה והשתלת מח עצם עצמית, ואלה השיגו הפוגה של חצי שנה בלבד לפני שהמחלה חזרה לתקוף באגרסיביות. גם טיפול כימותרפי נוסף לא הועיל, והמחלה המשיכה להתפשט ואף לא איפשרה השתלת מח עצם מתורם. משלא נמצא פיתרון אחר, הופנה אמיר לשיבא ועבר את הטיפול הייחודי.
התוצאה: כמו קסם, כעבור חודש בלבד הראו הבדיקות שהגוף התנקה מהסרטן. "בימים הראשונים אחרי החדרת התאים אמנם פיתחתי חום גבוה, אבל לא הגעתי למצב סוער כמו חלק מהמטופלים שעוברים את התהליך", הוא סיפר. "כיום כבר אין מחלה פעילה ואין ממצאים פתולוגיים".
החיים יקרים
הטיפול המהפכני, שזכה כבר לאין ספור פרסומים בכתבי עת מדעיים וגם בתקשורת המיינסטרים, עובד כיום בעיקר בסוגים שונים של סרטני דם משום שבגידולים כמו לוקמיה או לימפומה, קל יחסית לתאים המהונדסים לתקוף את תאי הסרטן שנוכחים בזרם הדם.
כיום מתנהלים ניסויים קליניים שונים לבדוק את יעילות השיטה גם נגד גידולים שונים. לפני חודשים אחדים פורסם על ניסוי שנערך על ידי חוקרים מאוניברסיטת פנסילבניה ובית החולים הכללי של מסצ'וסטס, בעשרה חולים סופניים בסרטן מוח מסוג גליובלסטומה רב צורנית.
החולים בניסוי הזה שרדו בממוצע כתשעה חודשים לאחר תחילת הטיפול – זמן רב באופן משמעותי לעומת התחזיות, בשל מצבם וסוג הסרטן האלים מאוד שמהם סבלו. אצל אף אחד מהם הגידול לא נעלם לחלוטין, אבל אצל מקצתם המחלה התייצבה ולא חלה הידרדרות במשך תקופה.
טכנולוגיה טיפולית דומה נמצאת בשימוש של חברת קייט פארמה הישראלית, שנרכשה לאחרונה על ידי חברת התרופות הענקית גיליאד סיאנסז. הטכנולוגיה של החברה מתבססת על מחקריהן של פרופ' זליג אשחר ממכון ויצמן, ופרופ' סטיבן רוזנברג מארצות-הברית. בשנה האחרונה היא עלתה לכותרות בזכות האקזיט הענק.
גם בבית החולים תל השומר מיישמים את הטכנולוגיה, לא באופן מסחרי. "טיפלנו עד היום בארבעים וחמישה חולים", אומר פרופ' ארנון נגלר. "רובם עם לימפומה, והשאר עם לוקמיה לימפטית חריפה. רובם המוחלט ילדים, ושלושה מבוגרים".
גם במקרה הזה, התוצאות יוצאות דופן. בלימפומה הושגה תגובה ב-70% מהחולים, וריפוי ב-40% מהם. "אלה חולים שבלי הקאר סביר להניח שהם היו נפטרים. כלומר, מדובר באנשים שמיצו כל טיפול אחר, והמחלה שלהם הראתה יציבות ולא הושפעה מהטיפול. הקאר הציל את חייהם".
ה"קאר" שבו מטפלים בשיבא הוא "CD28", והוא נמצא בשימוש תחת פיקוח של ועדת הלסינקי. כלומר, כטיפול חמלה בלבד ולא באופן מסחרי. מכיוון שכך, הוא ניתן אך ורק לאנשים שאיבדו כל תקווה אחרת. מאז שהוכנס לשימוש, התקבלו בשיבא פניות מכל רחבי הארץ ומספר המאושפזים המטופלים בטכנולוגיה עולה.
שתי הטכנולוגיות המסחריות לא נמצאות בסל התרופות בישראל ועל כן לחולים שאינם בעלי אמצעים אין כל יכולת להשיג את הטיפול אלא במסגרת מחקר. אפשר לנסות לעבור את הטיפול באחד מעשרות המרכזים הרפואיים הרלוונטיים בארצות הברית, אבל המחיר כמעט דמיוני – כ-400 אלף דולר בממוצע.
"נכון, יש ביקורת על המחיר, אבל אם מנתחים את הנתונים מבינים שהעלות היא לגמרי לא יותר גבוהה מטיפולים אחרים בשוק, שיעילים פחות", מסביר אוסטני מחברת נוברטיס. "אל תשכח שמדובר בטיפול חד פעמי, וזהו ערך משמעותי לחולה, הוא יכול לחזור לחיים נורמליים. כולנו יודעים איך נראים חייו של חולה סרטן, הם מתהפכים לחלוטין, שלא לדבר על משפחת החולה שגם חייה עוברים תהפוכות, וכאן זה נחסך. ויש גם ערך למערכת הבריאות - האפקטיביות של הטיפול. נכון לעכשיו, עלות הטיפול של התרופה המקובלת בקרב חולים אלו עומדת על 600-750 אלף דולר".
בארצות הברית, חברות הביטוח מכסות את עלות הטיפול וגם מערכת הבריאות הציבורית מגויסת. במקרים אחרים, חברות התרופות לוקחות על עצמן לממן את עלות הטיפול עבור חולים מסוימים. בישראל הטיפול עשוי לקבל אישור במהלך השנה הבאה, אך בשל מחירו אין לדעת האם ייכנס לסל התרופות.
הדור הבא / ד"ר אורי גרינבוים
אחד הכלים העוצמתיים ביותר למלחמה בסרטן הוא מערכת החיסון. בגופנו נוצרים תאים רבים בעלי פוטנציאל ממאיר, אך מערכת החיסון, ובעיקר תאי הT- שלה – יודעים לזהות את תאי הסרטן ולהשמיד אותם בטרם התפתחה המחלה. רק כשמתחמקים תאי הגידול ממערכת החיסון, יכול להתפתח סרטן.
אחת מפריצות הדרך החשובות של השנים האחרונות היא היכולת לגרום לתאי T של החולים לזהות תאי גידול, ולהשמיד אותם. אחד מהמפתחים הראשונים הוא חתן פרס ישראל פרופ' זליג אשחר, אשר הגה את הרעיון במעבדתו במכון ויצמן. בהמשך - עבר הפיתוח לארה"ב, ובשנה האחרונה אושר לראשונה הטיפול לשימוש מסחרי.
תאי ה-T נאספים מדם החולה, ובעזרת הנדסה גנטית מתוכנתים מחדש לבטא על התא קולטן המזהה את תאי המחלה, וגורם לתא ה-T להשמיד אותם. עד כה עיקר ההצלחות של הטיפול היו בלימפומה ולוקמיה של תאי B: תאי ה-T המהונדסים מוחזרים לחולה, מזהים את התאים הממאירים, מתרבים ומשמידים את תאי הגידול.
בהמשך חלק מהתאים נשארים כתאי זיכרון בגוף. המחקרים האחרונים מראים כי כחצי ויותר מהחולים, להם כבר לא היה כל טיפול אפשרי, מבריאים מטיפול חדשני זה. עדיין ישנם מכשולים במהלך הטיפול, הגורם לתגובה חיסונית עוצמתית, אך עם הזמן לומדים הרופאים לשלוט בתגובה זו, ולהימנע מנזק קשה למטופלים. בשלבי מחקר שונים נמצאים כעת מטרות נוספות על גידולים נוספים, ביניהם מיאלומה נפוצה, גליובלסטומה ועוד. אנו תקווה כי פריצת דרך זו תוכל להביא מזור לחולי סרטן רבים להם אין כיום אפשרות לטיפול מרפא למחלתם.
ד"ר אורי גריבוים - רופא בכיר במחלקה ההמטולוגית, בי"ח סורוקה מקבוצת כללית
בשיתוף סורוקה, מרכז רפואי אוניברסיטאי מקבוצת כללית
 לפנייה לכתב/ת
לפנייה לכתב/ת